安定成長期
スタチン
イノベーションに至る経緯
(コンパクチンの発見)
三共でのコレステロール合成阻害剤の研究は、1971年ごろより開始されたが、中心的な役割を果たしたのは当時三共の発酵研究所に勤めていた遠藤である。
遠藤は米国留学中に帰国後の研究テーマについて検討し、「米国の研究者と競合する研究をしても絶対に勝ち目のないことがよく分かった。筆者のような留学生の中には、帰国後も留学中のテーマかその周辺のテーマを研究する人が少なくなかったが、そのようなやり方では、落ち穂拾いか、米国の研究者の引き立て役にしかなれなかった。苦労してでも、彼らと競合しない、独自のジャンルを切り開くしかないという結論に達した」と述べている1。
遠藤は、ヒトでは大半のコレステロールが体内で合成されることに着目し、コレステロールの体内への吸収を阻害するよりも、体内での合成、特に律速酵素「HMG-CoA 還元酵素」を阻害すれば、血中コレステロールが効果的に下がると予測した。また「カビとキノコの中には他の微生物との生存競争に打ち勝つための武器として、コレステロールの合成阻害物質を作るものが存在する」という仮説に基づき、1971年、カビとキノコの中にあるコレステロール合成阻害物質の探索を開始した。
遠藤は、2年にわたり約6000株の青かび等微生物のスクリーニングを行い、青かびが産み出すコンパクチン(ML-236B)というHMG-CoA 還元酵素阻害物質を発見した。1974年に特許出願、次いで1974年から1976年にかけてラットを使ったコンパクチンの非臨床試験を実施した。しかし、ラットには血清コレステロール低下作用が起きなかった。そこで、毎日卵を産み血中コレステロールの高い産卵鶏を使ってみると、これは劇的な効果を示すところとなった。非臨床試験は犬等他の動物にも広げられコンパクチンの効果を明らかにしていった。この成果は米国では1975年5月に出願(物質特許)され、1976年9月に登録されている。また、この発見に関する最初の論文二編は1976年12月に公刊された2,3。
(国際共同研究と医薬品化への挑戦)
血液中でコレステロールはLDLあるいはHDLといったリポタンパク粒子に組み込まれて存在し、組織に輸送される。その後の研究で、コンパクチンをはじめとするスタチンが下げるのは、動脈硬化の原因となる悪玉のLDLコレステロールであることがわかった。スタチンの作用メカニズムが明らかにされて医薬品として成功するまでの過程には、遠藤らの三共グループとブラウンとゴールドスタインとの国際共同研究が大きく貢献している。
ブラウンとゴールドスタインは1976年、遠藤に共同研究を提案してきた4。彼らは、遠藤らのコンパクチン発見とほぼ同時期の1973年に、LDLを循環血液中から細胞に取り込む働きをするLDL受容体を発見していた。加えて、細胞にはコレステロール量を常に一定に保つフィードバック制御と呼ばれる仕組みがあり、細胞にコレステロールが十分にあると、コレステロールの合成とともにLDLの受容体による取り込みが抑制される現象を見いだしていた(図1(1))。そこで、コンパクチンを細胞に加えてコレステロール合成を抑制すれば、合成量の低下を補うために、HMG-CoA 還元酵素とともにLDL受容体も増加すると予測し、実証したのである(図1(2))。この共同研究により、コンパクチンは細胞へのLDL取り込みを増大する結果、血中LDLコレステロールの低下がもたらされるメカニズムが明確になってきた。
しかし、当時、遠藤をはじめとする三共の研究チームは、大きな課題に直面していた。コンパクチンを投与されたラットに肝毒症の症状が出たのである。しかし、コンパクチンの有効性は大阪大学の山本章によって家族性高コレステロール血症(FH)の重篤患者に投与することでも証明され5、臨床試験は続行された。
このような、遠藤やゴールドスタインらの研究成果に触発され、各国科学者、製薬会社の間では医薬品としてのスタチン開発の研究が盛んになっていた。
1976年以来、アメリカの大手製薬企業・メルク(MSD)社は、遠藤からコンパクチンに関するサンプルやデータの提供を受けながら独自に研究開発を進めていた。そして、1978年にはコウジカビの一種 (Aspergillus terreus) から新たなスタチンであるロバスタチンを分離することに成功した6。
遠藤は1978年に三共を去って東京農工大学に異動した。三共のチームは更なる試験を続け製品化の途を探っていた。しかし、1980年、再びスタチンの毒性に関する試験結果が示された。ビーグル犬での2年間連日投与試験において、高投与量群に約半数の割合で腸管にリンパ腫様症状が観察されたのである。三共はコンパクチンによる製品化を一時的に断念せざるを得なくなった。これはメルクなど他の機関にも影響を与えた。
しかし1年後、金沢大学の馬渕宏はコンパクチンがFHヘテロ型の高コレステロール血症患者の血中LDL を低下させることを示した7。 ブラウンとゴールドスタインは、イヌにロバスタチンを投与し、「肝臓のコレステロール低下を補うためにLDL受容体が増加し、血中からのLDL取り込みが促進される結果、LDLコレステロールの顕著な低下をもたらす」スタチンの作用メカニズムを実験的に証明した8。この論文は、高LDLコレステロール血症の治療にHMG-CoA還元酵素阻害薬を用いることへの科学的根拠を提供することとなった9。これらの発表は、大きな反響を呼んだ。ビーグル犬での試験結果から開発をためらっていたメルクや三共は、これらの結果によって再びそれぞれが開発したスタチンの医薬品化に挑戦を開始することとなった。
図1 スタチンが血中LDLコレステロールを低下させるメカニズム
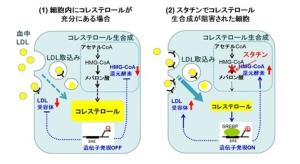
細胞内のコレステロール量は「フィードバック制御」により常に一定に保たれており、(1)細胞内にコレステロールが充分にあると、遺伝子スイッチがOFFになり、コレステロール生合成(HMG-CoA還元酵素)とLDLの取り込み(LDL受容体)が抑制される。(2)スタチンによりコレステロール生合成が阻害されると、低下を補うために遺伝子スイッチがONになり、HMG-CoA還元酵素とともにLDL受容体が増加し、細胞へのLDL取り込みを促進する。その結果、血中LDLコレステロールが効果的に低下する(SRE:ステロールによって調節される遺伝子の調節領域の応答配列;SREBP:HMG-CoA合成酵素などDREに統合するタンパク質)。
(製品化)
メルク社が開発したロバスタチンはその後の臨床試験で、安全性が比較的高く、優れたコレステロール低下作用を持つことが示されるところとなった。既に1979年2月には結晶の単離が行われ、6月に特許出願されていた10。ロバスタチンは、 遠藤がほぼ同時に発明し特許権を有したモナコリンKと同一の物質であったが、同社の製品化は1987年で、これが世界で初の製品化されたスタチンとなった。
ロバスタチンの製品化から2年後の1989年、三共はプラバスタチンの開発、製品化に成功した。これは、コンパクチンをイヌに投与し尿中活性代謝物を調べる実験を行ったところ、コンパクチンより活性及び標的臓器への選択性が優れた新たなスタチンを見いだしたのである11。分離精製が実施され、1980年6月に特許出願が行われた12。ビーグル犬の臨床結果によるコンパクチンの開発中止を経て、新たに見いだされたプラバスタチンは1981年,三共の 第一開発候補物質に選択された13。 プラバスタチンが水溶性を有すること、また肝細胞選択的であることは、安全性に貢献すると考えられたためである。前臨床試験が1981年より開始された14。
構造解析の結果、プラバスタチンはコンパクチンのデカリン骨格のC6β位に水酸基が導入された化合物であり、コンパクチンに比べ試験管内実験で10倍の阻害活性があることが明らかになった。プラバスタチンはコンパクチンの代謝物であり、製品化にあたってはコンパクチンからの効率的な生産方法を確立する必要があった。 当初は化学合成法により生産することが検討されたが、収率が低いことが確認された。 そこで、大量生産体制を確立するため、以下に述べるように、微生物による変換により生産するプロセスの研究開発は「非常に緊急性の高いテーマ」として実施され、短期間に成功を収めることができた。この研究開発の結果、プラバスタチンの大量生産を行うため、(1) 青カビ Penicillium citrinum SANK 11480株)からコンパクチンを発酵生産し、続いて (2) 放線菌 Streptomyces carbophilus(SANK 62585)の変換酵素であるチトクローム P-450 を用いてコンパクチンナトリウム塩(ML-236B-Na)の6β位に水酸基を導入するプラバスタチンへの変換発酵を行う二段階発酵プロセスが採用された。プラバスタチンの二段階発酵生産プロセスに対応した生産設備を構築するため、1984年6月に三共は福島県小名浜に用地を取得し、工場建設を開始した。1987年3月に工場は開設された。その後、1987年4月には第二期工事を開始し、1988年9月、コンピュータ設備を備えたプラバスタチンの発酵・抽出生成工場が竣工した。プラバスタチンの第Ⅰ相臨床試験は1984年3月開始され、同年5月に完了した。また、高脂血症患者を対象とした二重盲検法による第Ⅰ相臨床試験は1984年9月に開始され、翌1985年1月に完了した。
日本初の上市されたスタチンであるプラバスタチンの特性として、親水性を有することによりコレステロール生合成を阻害するスタチンの作用機序において重要な、肝臓系への組織選択性を有することが挙げられる。ロバスタチンやシンバスタチンなどがコレステロール合成の主要臓器である肝臓や小腸のみならず他の臓器でも高い阻害活性を示す一方、プラバスタチンは肝臓や小腸でのコレステロール合成を強く阻害する点で異なっている。
(第2世代のスタチン)
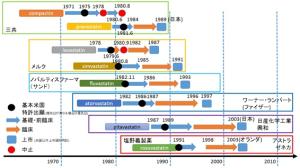
HMG-CoA 還元酵素の阻害を主な作用機序とした医薬品は三共とメルクに続き、世界の多くの製薬企業でも研究開発が行われ次々と新製品が生み出された。コンパクチン、プラバスタチン、ロバスタチン及びシンバスタチン以降のスタチン類は、ファイザーやアストラゼネカなど、三共、メルク以外の企業が研究開発に成功した。これらのスタチンには、コンパクチンと同じく天然物から探索されたもの(ロバスタチン)、それを改良したもの(プラバスタチン及びシンバスタチン)、完全に合成されたもの(フルバスタチン、アトロバスタチン、ピタバスタチン、及びロスバスタチン)がある。全てのスタチンはコンパクチンと同じメバロン酸類似の基本骨格を有している。結果、2014年現在までに合計8種類のスタチンが市場に投入された (図4参照、なお図中には明記していないが一種類[セリバスタチン; cerivastatin] は安全性の問題により2001年販売停止された)。
スタチン類の上市後最初の10年間は、市場参入が最も早かったメルク(ロバスタチン及びシンバスタチン)と三共(プラバスタチン)が市場のほとんどを占有した。
その後、スタチンのノン・ジェネリック市場の成長を支えたのは、ワーナー・ランバート (現・ファイザー) が開発した、アトルバスタチン (リピトール) である。アトルバスタチンは完全合成であり、従来のスタチンと比較して強度が格段に強く「スーパースタチン」と呼ばれる。2000年代の後半では別の「スーパースタチン」で、塩野義製薬が探索し、最終的にはアストラゼネカが開発したロスバスタチン(クレストール)が、売り上げ及びシェアを大きく伸ばしている。ロスバスタチンも完全合成スタチンである。スーパースタチンを発明したのは、先行企業の三共とメルクではなく、全く別の創薬企業であった。このことは、知識の公開とそれによる多様な研究開発主体の参入が産業のイノベーションのパフォーマンスを高めてきたことを示唆している。